Читать книгу "Функциональная анатомия лимфатической cистемы"

Автор книги: Валерий Петренко
Жанр: Прочая образовательная литература, Наука и Образование
Возрастные ограничения: 16+
сообщить о неприемлемом содержимом
Валерий Петренко
Функциональная анатомия лимфатической cистемы
Введение
Сегодня в России и во всем мире проводятся активные исследования в области лимфологии. Лимфология – это наука о лимфатической системе, о ее строении, функциях и развитии, ее месте в организме индивида. Классическая, фундаментальная лимфология возникла в XX веке. Она «выросла» из функциональной анатомии лимфатической системы, которая изучает строение лимфатической системы в связи с ее функциями, в т.ч. в развитии. Именно анатомы, начиная от O. Rudbeck и Т.Bartolinus (XVII век), сформировали классические представления о лимфатической системе как системе лимфатических сосудов и узлов. Позднее к ним присоединились другие морфологи, физиологи и клиницисты. В XX веке Д.А. Жданов (1940) написал: «…лимфатическая система в ее структурах и функциях является во многих отношениях решающей базой, на которой разыгрываются процессы обмена веществ, развертываются реакции организма на инфекцию, распространяются новообразования… Лимфоузлы являются биологическими и механическими фильтрами для протекающей сквозь узлы лимфы».
Фундаментальная лимфология имеет две составляющие – морфологическую и физиологическую, они тесно взаимосвязаны. На основе фундаментальной лимфологии возникла клиническая лимфология. Ситуация известная: анатомия и физиология являются базовыми научными дисциплинами, азбукой медицины. Ее частью стала современная лимфология – интегративная медико-биологическая наука, которая связана с такими совсем еще молодыми науками, как иммунология и клеточная биология.
Анатомия лимфатической системы является одним из наиболее интересных в теоретическом плане, очень важных в прикладном отношении и одновременно сложных разделов анатомии человека. Лимфатическое русло дополняет вены в дренировании органов, снимая с вен часть функциональной нагрузки. Кроме «избыточной» тканевой жидкости в виде лимфы, в корни лимфатической системы поступают крупнодисперсные частицы и клетки, в том числе опухолевые. А следовательно, чрезвычайно важными для прикладной медицины становятся подробные знания о вариабельных путях лимфооттока из всех органов и областей тела человека. Лимфатическая система тесно связана с лимфоидными (иммунными) органами, особенно вторичными (периферическими) и, таким образом, играет очень важную роль в формировании и поддержании иммунитета. Знание основных этапов и критических периодов индивидуального развития лимфатической системы, сроков ее закладки, основных процессов и механизмов сложного морфогенеза безусловно необходимо для будущего врача, поскольку без этого невозможно сформировать правильные представления о нормальном строении лимфатической системы человека во всем разнообразии индивидуальных вариантов, его становлении, возникновении врожденных аномалий лимфатической системы, планировать и осуществлять эффективную профилактику, диагностику и коррекцию связанных с этим отклонений в развитии человека. Однако для рассмотрения строения, топографии и развития лимфатической системы на кафедре анатомии человека отводится крайне мало учебного времени, главным образом в рамках лекционного курса и самостоятельной внеаудиторной работы студентов. В существующих учебниках по анатомии человека эти вопросы освещены недостаточно, нередко с ошибками, многие сведения устарели. На кафедре гистологии и эмбриологии студенты изучают главным образом строение лимфатических узлов и других лимфоидных органов.
Лимфатическая система является одной из наиболее труднодоступных для изучения систем, но играет очень важную роль в жизнедеятельности организма: она структурно объединяет межклеточные пространства и кровеносную систему в единую циркуляционную систему его внутренней среды, регулирует переход межклеточной жидкости в кровь (от клеток к органам). В последние полвека бурное развитие получила клиническая лимфология, которая использует данные по анатомии и физиологии лимфатической и лимфоидной систем. Врачи активно борются с такими тяжелыми заболеваниями, как опухоли и их метастазы, лимфедема, разрабатывают разные методы их диагностики (лимфография) и лечения (эндолимфатическая терапия, введение лекарственных препаратов в грудной проток, лимфосорбция и др.), рациональные оперативные доступы к лимфатическим коллекторам и узлам.
Еще в IV–III веке до н. э. греческие ученые из Александрийской школы врачей Герофил и Эразистрат описали лимфатические сосуды и узлы в брыжейке тонкой кишки. Их работы были незаслуженно надолго забыты. В XVII веке н.э. G. Asellius (1622) вновь открыл лимфатические сосуды в брыжейке тонкой кишки собаки. Не зная реального значения сосуда, в 1563 г. B. Evstachii описал грудной проток у лошади под названием белой грудной вены. J. Pequet (1651) нашел брыжеечные лимфатические сосуды и грудной проток у собаки, T. Bartolinus (1652) – у человека. Новый период в истории изучения грудного протока и его корней начался в 1693 г., когда A. Nuck опубликовал описание метода инъекции лимфатических сосудов ртутью. G. Aselius (1627) и W. Hewson (1774) выделили истинные лимфатические узлы у человека и млекопитающих животных.
В ХVII веке O. Rudbeck и Т.Bartolinus впервые стали рассматривать лимфатические сосуды и узлы как отдельную систему, лимфатическую – самостоятельную совокупность особых анатомических образований, со специфичными строением и функциями. В первой половине ХVIII века появился целый ряд описаний вариантов и аномалий строения грудного протока и его корней. В ХVII–ХVIII веках лимфатическую систему изучали преимущественно путем препарирования и все чаще после предварительной инъекции каких либо составов: в ХVII веке был изобретен шприц, который все чаще стали использовать для инъекции лимфатического русла. В XIX веке для морфологических исследований стали применять формалин с целью фиксации материала, что позволило его уплотнять и предупреждать его разложение. Это ускорило развитие анатомии, особенно микроскопической, гистологии и эмбриологии. Внедрение в практику морфологических исследований формалина произвело революцию в науке, сопоставимую с началом использования примерно в это же время хлороформа в хирургии: стало возможным изучать структурные основы лимфотока.
Лимфоток из разных органов и областей тела человека и животных совершается в вены, причем не только пассивно. Лимфатические сосуды и узлы обладают способностью сокращаться благодаря собственным гладкомышечным клеткам и таким образом поддерживать скорость лимфотока, клапаны определяют его направление и сегментарное строение лимфатических сосудов. L. Ranvier (1875–1882) обозначал их луковицеобразные расширения с миоцитами в стенках над клапанами как «лимфатические сердца», W. Pfuhl (1939) – как «микролимфатические сердца», скопления миоцитов в их стенках – как мышечные манжетки. Миоциты образуют морфологическую основу функциональной автоматии лимфатических сердец: эти транспортные сегменты лимфатического сосуда между соседними клапанами (Webb R., 1932; Webb R., Nicol P., 1944) поочередно сокращаются и продвигают лимфу к венам. E. Horstmann (1951) предложил выделять функциональную единицу лимфатического сосуда – его клапанный сегмент: дистальный из двух соседних клапанов, в основании которых мало или нет миоцитов, и проксимально присоединяющаяся мышечная манжетка. Такое неравномерное строение лимфатического сосуда с чередованием клапанов и мышечных манжеток соответствует колебательному, толчкообразному лимфотоку. H. Mislin (1961) экспериментально подтвердил эту мысль и предложил новое название клапанному сегменту – «лимфангион»: он работает как мышечный насос даже в изолированных фрагментах (биоптатах) лимфатического сосуда. Функциональная автоматия сокращений лимфангионов имеет как миогенную, так и эндотелиальную природу, состояние сосудистой стенки зависит от состава лимфы и характеристик лимфотока. R. Schipp (1965, 1967) и H.J. Oemke (1968) подробно исследовали субмикроскопическое строение всех оболочек и частей лимфатического сосуда. R. Schipp показал важную роль нервных структур в регуляции сокращений лимфангионов: они концентрируются в области мышечной манжетки. В настоящее время проводится поиск в стенках лимфангионов пейсмекерных структур, запускающих сокращения лимфангионов (McCloskey K.D. et al., 2002).
Отечественные ученые внесли важный вклад в исследования лимфатической системы. Так Н.Ф. Высоцкий (1877) первым применил с этой целью тушь, А.С. Золотухин (1927) – рентгеновские лучи. Профессор Г.М. Иосифов (1904, 1914) впервые подробно описал у человека строение и положение начального отдела грудного протока и его корней, отметил влияние на лимфоток в них дыхательных экскурсий диафрагмы. Его книга «Лиматическая система человека с описанием аденоидов и органов движения лимфы» (1914) сыграла важную роль в развитии отечественной лимфологии и была переведена на немецкий язык. Г.М. Иосифов и И.М. Иосифов провели многочисленные исследования видовых особенностей строения лимфатической системы у позвоночных животных разных классов и видов. Ученик Г.М. Иосифова, академик АМН СССР Д.А. Жданов (1945, 1952) подробно изучил варианты внешнего строения и топографии грудного протока, поясничных и кишечного стволов, лимфоузлов на обширном трупном материале человека. Д.А. Жданов впервые показал, что постоянными корнями грудного протока у человека служат поясничные стволы, а кишечный ствол является непостоянным притоком грудного протока или поясничных стволов. Он и профессор М.Г. Привес в 30– е годы XX столетия использовали методики рентгенолимфографии для прижизненного наблюдения строения, положения и движений грудного протока. Вместе со своими учениками Д.А. Жданов подробно изучил анатомию лимфатического русла разных внутренних органов и кожи. Наиболее известная его монография «Анатомия и физиология лимфатической системы» (1952) до сих пор служит настольной книгой лимфологов. Академик АМН СССР В.В. Куприянов предложил термин «лимфатический посткапилляр» и описал его строение. Академики АМН СССР М.Р. Сапин и Ю.И. Бородин, их ученики исследовали функциональную морфологию и топографию лимфоузлов разных групп и областей у человека и млекопитающих животных. М.Р. Сапин отводит ключевое место в составе лимфатической системы лимфоузлам как лимфоидным органам, в которые лимфатические сосуды приносят периферическую лимфу для фильтрации. М.Р. Сапин считает, что лимфатическая система является частью лимфоидной (иммунной) системы, М.Г. Привес – наоборот. Ю.И. Бородин предложил концепцию «лимфатического региона» (лимфоузел и пути оттока лимфы из органов), создал и стал в 1991 г. первым директором Института клинической и экспериментальной лимфологии в Новосибирске. Профессор А.В. Борисов способствовал распространению в СССР концепции E. Horstmann и H. Mislin о лимфангионе как клапанном сегменте лимфатического сосуда. Профессор В.М. Петренко обосновал строение лимфангиона как межклапанного сегмента лимфатического сосуда, в состав которого входит не только дистальный (входной), но и выходной, проксимальный клапаны лимфангиона: в целом организме и в биоптатах лимфатических сосудов лимфангион с одним клапаном не сокращается, а его мышечная манжетка соединяется с обоими клапанами посредством мышечных пучков. Разнообразные мышечные связи соседних лимфангионов способствуют координации их сокращений. В.М. Петренко впервые предложил рассматривать лимфатические узлы как лимфангионы лимфоидного типа (с лимфоидной тканью в стенках), лимфатическое русло – как непрерывную цепь межклапанных сегментов с разным строением, в т.ч. безмышечных, которые организуют парциальный лимфооток из органов в вены. В.М. Петренко опроверг бытовавшее мнение о только пассивном движении клапанных створок в лимфатических сосудах, с использованием гисто– и иммуногистохимических методик исследования, электронной микроскопии доказал наличие собственных гладких миоцитов в створках клапанов. Формирование лимфатических сосудов и узлов человека и позвоночных животных он рассматривает в тесной связи с органогенезом, с позиций генетического единства лимфатической и кровеносной систем. Это позволило объяснить механизмы становления вариантов нормального строения лимфатической системы человека и возникновения ее аномалий. В.М. Петренко на основе полученных данных о строении и развитии лимфатической системы предложил концепцию о ее конституции – общем сегментарном устройстве с соответствующими особенностями функционирования, а также концепцию о лимфоидно-лимфатическом аппарате – анатомической основе иммунитета человека.
Судьба по своему распоряжается путями развития лимфологии. Так Г.М. Иосифов в 1894 г. окончил медицинский факультет Харьковского университета и был оставлен помощником прозектора на кафедре нормальной анатомии. В 1899 г. Г.М. Иосифов защитил диссертацию на тему: «К вопросу о нервах glandulae thymus у человека». Он первым провел статистически достоверное исследование (на 40 трупах взрослых людей) строения и топографии начального отдела грудного протока и показал, что по мере повышения уровня формирования грудного протока от I–II поясничных до XII–ХI грудных позвонков цистерна в его начальном отделе вытесняется цистерной и сплетением поясничных стволов («Начало грудного протока и его расширение»: Труды научного общества Харьковского медицинского института, 1904). Эти данные использовали в своих работах такие известные анатомы, как H. Rouviere (1932) и Д.А. Жданов (1945). В 1904–1906 гг. Гордей Максимович находился в заграничной командировке – работал в анатомических институтах и музеях Мюнхена, Цюриха, Павеи и Парижа. В 1906 г. профессор Г.М. Иосифов был избран заведующим кафедрой нормальной анатомии Томского университета, в 1923 г. – Воронежского университета (позднее – медицинского института). Г.М. Иосифов проводил научные исследования по анатомии лимфатической системы у человека и позвоночных животных. Самым известным научным трудом Г.М. Иосифова стала книга «Лимфатическая система человека с описанием аденоидов и органов движения лимфы» (Томск, 1914), где описаны: 1) строение лимфатической системы, 2) ее развитие в филогенезе и онтогенезе позвоночных животных, 3) структурные основы лимфотока. В 1930 г. эта же книга вышла на немецком языке в Йене. Сохранило научное значение представление Г.М. Иосифова о пассивном лимфатическом сердце (цистерна грудного протока в связи с поясничными ножками диафрагмы).
Под началом профессора Г.М. Иосифова начинал свой путь в науку Д.А. Жданов, еще студентом Воронежского мединститута. Затем он стал заведующим кафедрой нормальной анатомии в Горьковском мединституте, где защитил докторскую диссертацию (1943) и написал первые две монографии – «Функциональная анатомия лимфатической системы» (1940) и «Хирургическая анатомия грудного протока и главных лимфатических коллекторов и узлов туловища» (1945). В 1943 г. Д.А. Жданов стал директором Томского мединститута, в 1946 г. – II Ленинградского мединститута, который под его руководством был преобразован в Ленинградский санитарно-гигиенический мединститут. Д.А. Жданов стал основателем новой научной школы анатомов-лимфологов в ЛСГМИ и здесь написал третью большую монографию «Общая анатомия и физиология лимфатической системы» (1952). С 1956 г. Д.А. Жданов заведовал кафедрой нормальной анатомии в I Московском мединституте, где одним из его учеников был будущий академик М.Р. Сапин.
В Москве Д.А. Жданов продолжил руководить исследованиями анатомии лимфатического русла разных органов, включая вопросы иннервации, начал исследования анатомии лимфоузлов. Академик Д.А. Жданов был председателем Всесоюзного общества анатомов, гистологов и эмбриологов, Президентом Всемирного Конгресса Анатомов.
В 1932–1935 гг. кафедрой нормальной анатомии учебного комплекса «медвуз – больница имени И.И. Мечникова – техникум» с вечерней формой обучения (в 1935 г. комплекс вошел в состав II ЛМИ) заведовал профессор Н.Д. Бушмакин. Он закончил Казанский университет, где под руководством В.Н. Тонкова защитил диссертацию по лимфоузлам. Позднее заведовал кафедрами нормальной анатомии в Варшаве, Ростове, Казани, Иркутске, Хабаровске, был организатором мединститутов в Иркутске и Хабаровске, заместителем директора ВИЭМ по научной работе в Ленинграде.
Профессор К.В. Ромодановский также закончил медицинский факультет Казанского университета, там же начинал путь в науку, заведовал кафедрами нормальной анатомии в Омском, Ленинградском педиатрическом, Сталинабадском и Новосибирском мединститутах. Одним из направлений научных исследований К.В. Ромодановского была анатомия лимфатической системы. Среди его учеников – академик Ю.И. Бородин.
Общая анатомия лимфатической системы
Сердечно-сосудистая система организует межорганную циркуляцию межклеточной жидкости по специальным каналам с собственными клеточными стенками – сосудам. В ее составе лимфатическая система («лимфа» / лат. – влага) осуществляет дополнительный, коллатеральный к венам и более медленный сосудистый дренаж органов, что облегчает переход крупных молекул и клеток в кровь. Лимфатические сосуды отводят избыток тканевой жидкости, основную массу крупнодисперсных частиц, коллоидов и лимфоцитов, которые не попадают в корни венозного русла, из органов в вены в виде лимфы. Хиломикроны (липопротеидные микрокомплексы) придают молочную окраску лимфе («хилус» / греч. – сок, млечный) в лимфатических сосудах тонкой кишки на высоте пищеварения. Лимфатические узлы, наряду с организацией лимфооттока, осуществляют очистку периферической лимфы от чужеродных веществ и клеток.
Лимфатическая система имеет следующие особенности строения: 1) корни лимфатического русла не связаны с кровеносным руслом, а следовательно – с сердцем, главным двигателем крови, поэтому скорость лимфотока, лимфатическое давление низкие (в лимфатических капиллярах – до 5–10 мм рт.ст., в кровеносных капиллярах – 20–30 мм рт.ст.); 2) лимфатическая система не замкнута в круг, ее корни начинаются слепо или образуют петли сетей без их прямого соединения с кровеносным руслом. Поэтому нет лимфообращения, лимфоотток из органов носит маятникообразный, колебательный характер, который в большей степени, чем кровоток, зависит от вспомагательных, внесосудистых факторов; 3) для строения лимфатического русла характерны клапаны – окружные складки стенки, выступающие в полость русла.

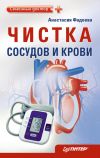
Схема организации сердечно-сосудистой системы: Ао – аорта; В – полая вена; ГМЦР – гемомикроциркуляторное русло; ЛК, ЛПК, ЛС, ЛУ – лимфатические капилляр, посткапилляр, сосуд и узел. Прерывистый эндотелиальный контур ЛК символи-зирует клапаноподобное устройство подвижных межэндотелиальных контактов
Они являются атрибутом всех лимфатических сосудов, кроме капилляров. Клапаны ограничивают обратный лимфоток; 4) «прерывистость» лимфатических путей – лимфатические узлы разделяют в экстраорганном лимфатическом русле афферентные и эфферентные лимфатические сосуды, являются функциональными анастомозами лимфатического и кровеносного русла: прямого перехода крови между ними в узлах нет, но через соединительную ткань между сосудами (интерстициальные каналы) возможны переход жидкости и миграция лимфоцитов. Лимфатические узлы выполняют депонирующую и резорбирующую функции – накопление и частичное всасывание лимфы в кровь.
Лимфатическая система имеет следующие основные звенья : 1) лимфатические капилляры; 2) лимфатические посткапилляры; 3) лимфатические сосуды; 4) лимфатические узлы; 5) лимфатические стволы; 6) лимфатические протоки.
Лимфатические капилляры – корни лимфатической системы. Они образуют трехмерные (объемные) и двухмерные (плоскостные) сети, в зависимости от конструкции органа. В местах соединения капилляров определяются их расширения (лакуны). Это способствует выполнению лимфокапиллярной сетью депонирующей функции. В некоторых органах в такой сети обнаруживаются пальцевидные, слепозамкнутые выросты (млечные синусы в кишечных ворсинках и др.).
Лимфатический капилляр, по сравнению с кровеносным, имеет ряд особенностей строения: 1) слепое начало (один конец замкнут или переходит в петлю сети капилляров); 2) более широкий просвет (20–200 мкм); 3) более тонкая эндотелиальная стенка (0,05–0,3 мкм); 4) извилистые очертания, поскольку отсутствует базальная мембрана. Это способствует прохождению крупных частиц и даже клеток в просвет лимфатического капилляра; 5) тонкие, обычно ретикулярные волоконца (стропные или «якорные» филаменты) соединяют лимфатический эндотелий с окружающими коллагеновыми волокнами. Эти «якоря» препятствуют сдавлению просвета лимфатического капилляра в случае большего гидростатического давления в окружающих тканях и способствуют их дренажу. Через временные и постоянные щели между эндотелиоцитами просвет лимфатических капилляров переходит в интерстициальные (предлимфатичетические) каналы – тканевые «щели», ячейки в густых сетях соединительнотканных волокон, заполненные коллоидом углеводов и белков (гликопротеины, протеогликаны), без собственной клеточной стенки и постоянного просвета. По ним, через подвижные контакты (внутристеночные миниклапаны) или сквозь эндотелиоциты (пиноцитозные пузырьки, трансцеллюлярные каналы) тканевая жидкость «стекает» в полость лимфатических капилляров с образованием лимфы.
Лимфатические и кровеносные микрососуды тесно переплетаются (разделены тонкими прослойками соединительной ткани с повышенным содержанием волокон), их функции сопряжены (специализация и кооперация соответственно разной проницаемости их стенок). Участки микроциркуляторного русла, прилежащие к магистральным артериоле и венуле, разделены их крупными ветвями на «микрорайоны». В их составе определяются «функциональные модули», чаще разветвленно-линейной конструкции – сети метаболических микрососудов (капилляры) между ветвями терминальной артериолы и корнями собирательной венулы. Иногда круговые пучки (спаренные анастомозы) этих транспортных микрососудов образуют кольцевые модули. Лимфатические капилляры проходят около кровеносных капилляров и посткапиллярных венул.
Лимфатические посткапилляры отличаются от лимфатических капилляров наличием в стенках: 1) лимфатических клапанов; 2) прерывистой базальной мембраны; 3) очень тонкого, непостоянного слоя рыхлой соединительной ткани. Лимфатические посткапилляры участвуют в резорбции интерстициальной жидкости и белков, могут формировать сети, часто сопровождают собирательные венулы. Клапаны разделяют лимфатические посткапилляры на межклапанные сегменты, его структурно-функциональные единицы.


Структурные основы лимфообразования (схема): подвижные межэндотелиальные контакты лимфатических капилляров устроены и функционируют как внутристеночные клапаны с подвижной внутренней и фиксированной (якорными филаметами) наружной «створками»
Они организуют пассивный лимфоотток из лимфокапиллярной сети благодаря клапанам. Стенки межклапанного сегмента сближаются под давлением наружной манжетки (паравазальные ткани) и выдавливают лимфу из его полости в обоих направлениях. Дистальный (входной) клапан ограничивает обратный лимфоток: клапанные синусы (промежутки между клапанными заслонками и стенками сосуда в виде карманов, открытых проксимально) заполняются лимфой, под ее давлением створки клапана сближаются и он закрывается. Прямой лимфоток раздвигает створки проксимального (выходного) клапана, устремляясь в следующий межклапанный сегмент. Клапан относится к обоим смежным сегментам лимфатического посткапилляра: он разделяет их полости (автономные компартменты), но объединяет их стенки, обеспечивая целостность микрососуда. Около магистральной артериолы и магистральной (мышечной) венулы или в составе их пучков (контур «микрорайона» микроциркуляторного русла) лимфатический посткапилляр переходит в лимфатический сосуд I порядка.

Ангиоархитектоника микроциркуляторного русла брыжейки тонкой кишки: МА, МВ – магистральные артериола и две венулы в одном пучке; ЛС – лимфатический сосуд; ТА – терминальная артериола; СВ – собирательная венула; ЛК и КК – лимфатические и кровеносные капилляры

Брыжейка тонкой кишки, тотальный препарат: 1 – клапаны отводящего лимфатического сосуда I порядка (лимфатического посткапилляра); 2 – клапан коллекторного лимфатического сосуда мышечного типа. Азотнокислое серебро

Микроциркуляторное русло в брыжейке тонкой кишки, гистологический срез: 1, 2 – лимфатические посткапилляры, проходящие в окружении сети соединительнотканных волокон и микрососудов; 3, 4 – пучок собирательной венулы и терминальной артериолы. Гематоксилин и пикрофуксин

Сосуды в брыжейке тонкой кишки, гистологический срез: 1 – клапан лимфатического посткапилляра; 2,3 – артериолы. Гематоксилин и пикрофуксин

Лимфатический капилляр почки: 1 – полость; 2–5 – клетки на разных этапах миг-рации через эндотелиальную стенку. Желез-ный гематоксилин

Лимфатический сосуд, инъецированный синей массой Герота: выраженные сужения на протяжении сосуда («перехваты») соответствуют местам прикрепления клапанов


Лимфатический сосуд, тотальный препараты, окрашенные галлоцианином. А (малое увеличение): видна цепь клапанов, над их заслонками сосуд расширяется в разной степени (клапанные синусы с разным наполнением). Б (большое увеличение): 1,2 – входной и выходной клапаны лимфангиона; 3 – область его мышечной манжетки.

Клапаны в полости вскрытого лимфатического сосуда (схема Sappey)

Клапан в полости лимфатического сосуда на тонком срезе. Гематоксилин и пикрофуксин

Kлапан крупного лимфатического сосуда на продольном срезе: 1,2 – эндотелий на аксиальной и париетальной поверхностях створки; 3 – складки пучков коллагеновых волокон; 4–4 – продольный мышечный пучок; 5 – ядра поперечных миоцитов. Гема-токсилин и пикрофуксин

Крупный лимфатический со-суд, область мышечной манжетки, продольный срез: Э – эндотелий; А – адвентиция (складчатые продольные пучки коллагеновых волокон); 1 – продольный мышечный слой интимы; 2 – циркулярные миоциты в средней оболочке; 3 – субадвентициальный продольный мышечный слой. Гематоксилин и пикрофуксин
Лимфатические сосуды диаметром 100–150 мкм в своей стенке, помимо эндотелия и рыхлой соединительной ткани, содержат гладкие мышечные клетки. В сосудах диаметром 200 мкм и более стенка ясно разделяется на три слоя, подобные оболочкам кровеносных сосудов, между ними наблюдается сгущение сети эластических волокон с образованием эластических мембран в крупных сосудах. В лимфатических сосудах морфологические границы между оболочками выражены гораздо хуже, чем в кровеносных сосудах, особенно это касается наружной эластической мембраны, которая прерывиста даже в грудном протоке. В субэндотелиальном слое тонкие ретикулярные, коллагеновые и эластические волокна преобладают, они формируют сети. В наружной оболочке более многочисленные и толстые коллагеновые волокна образуют складчатые пучки с преимущественно продольной ориентацией. При растяжении сосуда складки расправляются, чем увеличивается прочность сосудистой стенки. Миоциты распределяются неравномерно как на протяжении сосуда, так и в толще его стенки. В лимфатических протоках и крупных стволах они обнаруживаются во всех слоях стенки, на границах между оболочками у человека и крупных млекопитающих животных сети эластических волокон сгущаются с образованием эластических мембран, лучше выражена внутренняя мембрана. В лимфатических сосудах постоянно определяются клапаны. Они представляют собой круговые складки внутренних слоев сосудистой стенки, проникающие в полость сосуда и направленные проксимально (по ходу прямого лимфотока). В клапанной заслонке, обычно парной, выделяют утолщение в месте прикрепления к стенке (клапанный валик) и истонченную пластинку в полости (створка). Створка подвижна, воронкообразно изогнута. Пространство между створкой клапана и сосудистой стенкой – клапанный синус, его стенки очень тонкие, поэтому при наполнении синус выбухает («луковица»). Сужающийся в проксимальном направлении канал между заслонками клапана имеет форму воронки – аксиальный синус. Клапаны разделяют лимфатические сосуды на лимфангионы – отрезки между соседними клапанами, межклапанные сегменты, в стенках которых определяются гладкие миоциты.

Схема строения лимфангиона – межклапанного сегмента лимфатического сосуда (полость заполнена синей массой): КВ – клапанный валик, где сосредоточена основная масса миоцитов клапанной части сосуда; МСК – межстворчатый канал, который соединяет полости соседних лимфангионов; КС – клапанный синус; ММ – мышечная манжетка; АС – аксиальный синус
В лимфангионе можно выделить три части: стенки клапанного и аксиального синусов (области входного и выходного клапанов), мышечная манжетка. Мышечная манжетка, средняя часть межклапанного сегмента, постоянно и в наибольшем количестве содержит миоциты. Сокращения мышечной манжетки преодолевают сопротивление клапанов на пути прямого лимфотока, силы тяжести и других факторов, сдерживающих прямой лимфоток. Клапаны ограничивают обратный лимфоток. При большом содержании миоцитов в клапанном валике они образуют мышцу клапана. Напрягая заслонку клапана, она тормозит обратный лимфоток. Кроме того, мышца клапана способна изменять положение створок клапана и регулировать лимфоток между соседними лимфангионами. Таким образом, лимфангионы являются структурно-функциональными единицами лимфатического сосуда: мышечная манжетка и смежные клапаны (входной и выходной) в их взаимосвязи обеспечивают лимфоотток из органов.
Мышечные элементы сосудистой стенки являются важным фактором лимфотока, но не следует пренебрегать значением других факторов или лимфодвижущих сил. К ним относятся: 1) лимфообразование (гидростатическое и онкотическое давление тканей в окружении лимфатических капилляров); 2) механическое давление тканей и органов, окружающих лимфатические капилляры и сосуды, в т.ч. сокращение мышц; 3) дыхательные экскурсии диафрагмы, сопровождающиеся колебаниями внутригрудного и внутрибрюшного давлений; 4) эжекция (присасывающее действие) вен шеи.
Лимфатические сосуды имеют четковидную форму – участки их сужения, или «перехваты» (места прикрепления клапанов), чередуются с расширениями (клапанные синусы). Форма отражает периодичность, сегментарность строения лимфатического сосуда.
Лимфангионы имеют разную форму – шаровидную, эллипсовидную, цилиндрическую и др. Она зависит как от частоты размещения клапанов (длины межклапанного сегмента), так и от положения, размеров и строения стенок лимфангиона.
Внимание! Это не конец книги.
Если начало книги вам понравилось, то полную версию можно приобрести у нашего партнёра - распространителя легального контента. Поддержите автора!